Portaalsite voor de échte zeeaquariaan
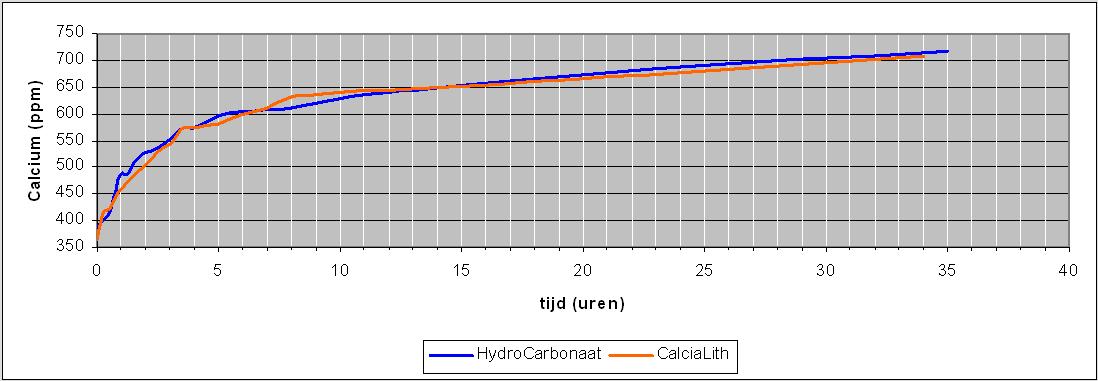
Optimale productie kalkreactor.
foto: Michael de Regt : Montipora digitata
Foto's Luc loyen.
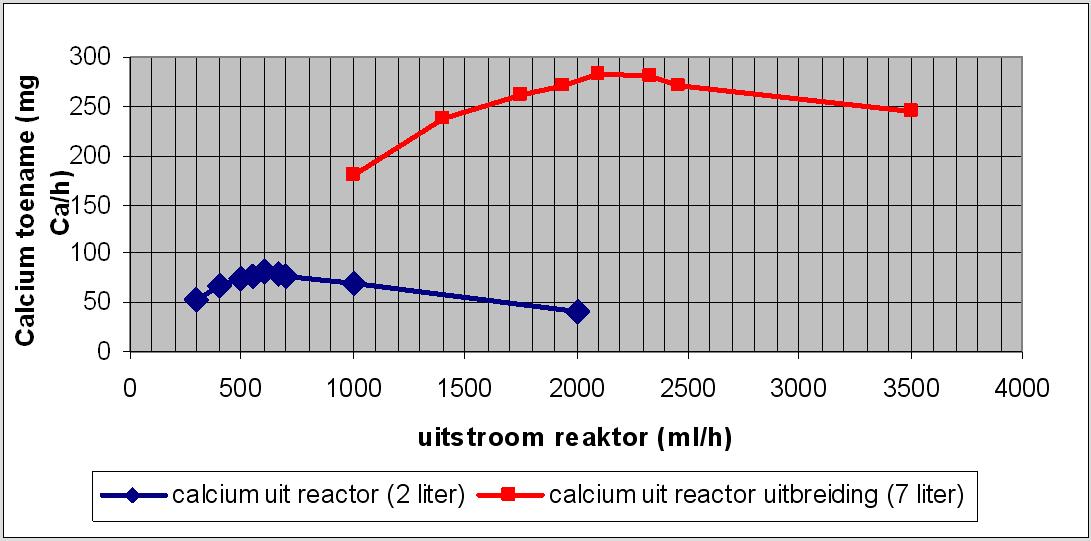
Het Zeeaquarium: Het rif als kalkreactor?
De cycli welke te zien zijn worden veroorzaakt door de afwisseling tussen zomer en winter op het noordelijk halfrond
(www.esrl.noaa.gov, modificatie).
op verschillende tijdstippen. Preind.:Preindustriële periode, S: gunstige prognose, I: worst-case scenario (gemodificeerd uit Orr et al, Nature, 2005).
B: solitaire poliepen, ontstaan na enkele maanden blootstelling aan zeewater met een gemiddelde pH van 7.4.
C Herstel door calcificatie van de kolonie na blootstelling aan normaal zeewater.
D: Tijdserie waarbij de procentuele verandering in proteïne/poliep en totaalgewicht van de kolonie is weergegeven.
Duidelijk is te zien dat bij een pH van 7.4 75% van het skelet verdwijnt, en dat binnen 4 maanden (gemodificeerd uit Fine et al, Science, 2006).
Balling methode: Toevoegingen aan het zeeaquarium.
In 70 ml gedestilleerd water is opgelost:
7 gr kaliumjodide (KI)
5 gr dijood (I2)
5 gr natriumacetaat
Natriumacetaat zorgt ervoor dat de jodium in het water opgelost blijft. Zuiver jodium lost zeer slecht op in water, maar als er al opgeloste jodium ionen in de oplossing voorkomen lost het verdere jodium makkelijk op door de vorming van polyiodidionen: I2 + I- → I3- + I2 → I5-
Lugol onderscheidt zich van jodiumtinctuur doordat jodiumtinctuur alcohol bevat en Lugol niet.
Wodka-methode Bestrijding van nitraat en fosfaat in het zeeaquarium
De Wodka-methode
Bestrijding van nitraat- en fosfaatoverschotten in het zeeaquarium.
Algenontwikkeling, bruinkleuring van kortpoliepige steenkoralen, achterblijvende groei, dagelijkse aanslag op de ruiten - veelgehoorde en regelmatig terugkerende problemen. Sommige ervan horen bij de opstart- of doorstartfase, andere horen bij de wat verder gevorderde bakken waarin met name de aquariaan zijn gevoel voor "evenwicht" kwijt is. De problemen kennen meerdere oorzaken en zijn in beginsel eenvoudig aan de bron aan te pakken. Het toepassen van de wodka-methode (of diverse andere trucjes) is slechts een lapmiddel, maar kan, mits het systeem in evenwicht verkeert een toegevoegde waarde leveren aan de kwaliteit van het aquarium.
1. Waar komen nitraat en fosfaat vandaan, waarom hopen ze op en welke problemen brengen ze met zich mee?
In vergelijking met natuurlijke riffen kennen onze aquaria een omgekeerde verhouding tussen producenten, consumenten en watervolume. Voor wat betreft het aantal koralen dat we huisvesten is dit nog niet zo’n groot probleem, het zijn eerder de aantallen vissen en de daaraan gerelateerde voedselbehoefte die voor problemen zorgen.
We voeren onze vissen groenvoer, vlokvoer, granulaatvoer en diepvriesvoer. Velen onder ons doseren voor de koralen diverse soorten vloeibaar voedsel, bijvoorbeeld aminozuren en andere “eiwitachtige” verbindingen. Een deel van deze stoffen wordt rechtstreeks opgenomen door het dierlijk leven. Een ander deel ‘verdwijnt’ ongebruikt in het systeem en wordt vervolgens – samen met de uitwerpselen van vissen, koralen en ongewervelden – grotendeels afgeschuimd. De rest van deze stoffen wordt opgenomen in de bacteriële assimilatie- en dissimilatieprocessen. Bij deze bacteriële omzettingen ontstaan als eindproduct nitraat en fosfaat. Dit proces wordt verderop toegelicht.
Nitraat en fosfaat maken onderdeel uit van respectievelijk de stikstofkringloop en de fosforkringloop. In onze aquaria stagneren deze ‘kringlopen’ bij nitraat (NO3-) en fosfaat (PO42-). Nitraat is en blijft in oplossing en wordt slechts spaarzaam, middels denitrificatie, omgezet in gasvormige stikstof (N2). Fosfaat is deels in oplossing en gaat deels een verbinding aan met calcium in kalkhoudende substraten zoals steen, zand, koraalgrit, maar ook koraalskelet. De bijdrage van bacteriologische defosfatering is verwaarloosbaar.
Hiermee ontstaan twee problemen tegelijkertijd:
(1) Nitraat en fosfaat vormen uitstekende nutriënten voor zoöxanthellen, algen en wieren. Een aquarium met een meetbare nitraatwaarde kent over het algemeen ook groei van algen en wieren. Indien een aantal geschikte algeneters aanwezig zijn is deze algengroei vaak niet zichtbaar of niet storend. Uitzondering hierop vormt het dagelijks ‘aanslaan’ van de ruiten. Daarnaast zorgt de aanwezigheid en beschikbaarheid van nitraat ook voor goede groei van zoöxanthellen met als gevolg dat de basiskleur van veel sps-koralen een min of meer bruinige ondertoon laat zien en gekleurde groeipunten klein of afwezig zijn doordat de zoöxanthellen de groei van het koraal kunnen bijhouden.
(2) Daarnaast zorgt de binding van fosfaat aan kalk ervoor dat de opbouw van het kalkskelet stagneert. De afzetting van calciumcarbonaat op calciumfosfaat functioneert slecht of helemaal niet, waardoor een steenkoraal zijn skelet niet verder kan uitbreiden.
2. Redfield-ratio: Waarom ontstaat ophoping?
Om te begrijpen waarom nitraat en fosfaat ophopen is een kort inzicht in de Redfield-ratio van belang. In 1934 ontdekte de Amerikaan Alfred C. Redfield dat de verhouding van koolstof (C), stikstof (N) en fosfor (P), in zeewater en zoöplankton in alle oceanen ongeveer gelijk is. Deze verhouding C:N:P bleek telkens weer rond de 106:16:1 te liggen. Dus 106 delen koolstof op 16 delen stikstof op 1 deel fosfor. Afwijkingen in de verhoudingen waren altijd kleiner dan 20%. Deze verhouding C:N:P van 106:16:1 wordt nu nog steeds naar zijn ontdekker de ‘Redfield’-ratio genoemd.
Latere studies hebben inmiddels uitgewezen dat niet sprake is van één soort plankton, net zo min als dat sprake is van één C:N:P-verhouding[1]. De Redfield-ratio blijkt een ‘gemiddelde’ verhouding te zijn. Voor de strekking van dit artikel kan bovengenoemde ratio als voorbeeld worden gehanteerd.
Voor de opbouw van biomassa van bacteriën, algen, wieren en zoöxanthellen wordt aangenomen dat de basisbouwstenen koolstof, stikstof en fosfor nodig zijn in de globale verhouding 106:16:1, ofwel, bij gebruik van 1 fosforatoom is behoefte aan 16 stikstofatomen en 106 koolstof atomen.
Waarom stoten bacteriën nitraat en fosfaat uit terwijl zij deze nodig hebben voor groei en vermeerdering? Alvorens deze vraag te beantwoorden wordt kort ingegaan op algengroei.
Algen, maar ook wieren en zoöxanthellen gebruiken fosfor (P) en stikstof (N) dat zij uit het water opnemen (of ontvangen van hun symbiosepartner) in de vorm van nitraat en fosfaat. Koolstof (C) betrekken zij uit opgelost CO2 (kooldioxide). Kooldioxide is over het algemeen onbeperkt beschikbaar. Teruggrijpend op de Redfield-ratio mag nu duidelijk zijn dat algen/wieren/zoöxanthellen (AWZ) in ons zeeaquarium onbeperkte groeimogelijkheden hebben; er is geen gebrek aan bouwstenen en de AWZ floreren.
In de zoetwateraquaristiek, waar plantengroei meestal zeer gewenst is, is het sturen op de nitraatconcentratie binnen de Redfield-ratio een manier om de ontwikkeling van planten te stimuleren en de ontwikkeling van algen te remmen.
In de zeewateraquaristiek is sturen op Redfield niet zinvol. Ten eerste is de groei van algen en wieren ongewenst. Ten tweede is sturen op Redfield bijna niet uitvoerbaar. Fosfor (in de vorm van fosfaat) dient bij voorkeur onmeetbaar te zijn. Daarbij mag dan volgens Redfield circa 16x zoveel stikstof (in de vorm van nitraat) tegenover staan. Gemeten met een Salifert testsetje kan tot 0,015 mg/l fosfaat worden bepaald, dit zou betekenen dat er omgerekend 0,16 mg/l nitraat aanwezig mag zijn[2]. Dergelijke lage waarden zijn met de thuis-test-sets niet nauwkeurig te bepalen.
Nu terug naar de vraag waarom bacteriën nitraat en fosfaat uitstoten. Bacteriën kunnen kooldioxide niet gebruiken als koolstofbron, hiervoor zijn zij afhankelijk van de eerder genoemde afvalstoffen, voedseloverschotten en detritus. Net als CO2 zijn deze laatste meestal in overvloed beschikbaar in onze aquaria. Deze voedingsbron kent één mankement: ze bevat te weinig koolstof in verhouding tot stikstof en fosfor. Ofwel, bij de assimilatie wordt het beschikbare koolstof (en in verhouding stikstof en fosfor) opgenomen, terwijl het overschot aan stikstof en fosfor aan zuurstof wordt gebonden en wordt uitgestoten als … nitraat en fosfaat.
3. Standaard maatregelen ter beperking van de ophoping van nitraat en fosfaat
Het ontstaan van nitraat en fosfaat is onvermijdelijk; deze problematiek wordt veroorzaakt door de samenstelling van de voeders die we beschikbaar hebben. Wat we wel kunnen doen is voorkomen dat de nitraat- en fosfaatoverschotten te groot worden.
Gemakshalve kan worden gesteld dat een gemiddeld aquarium verhoudingsgelijk (te) veel vis huisvest. Hierbij hoort een bepaalde inbreng van voedsel die uiteindelijk leidt tot een biologische belasting van het systeem - wat meestal in het voordeel van algen en wieren uitpakt. Met in achtneming van onderstaande aandachts- en onderhoudspunten moet het mogelijk zijn om de meetbare nitraatwaarde terug te brengen tot een waarde die lager ligt dan 5 à 10 mg/liter. Het is verstandig om fosfaat te verwijderen, met een fosfaatverwijderaar, tot een niet meetbare waarde met een gevoelige testset[3].
-
Door het voeren van vissen (en koralen) wordt het aquarium belast met organische stoffen, welke leiden tot een belasting met anorganische stoffen (nitraat, fosfaat). Des te minder men voert, des te minder afval de afschuimer hoeft te verwijderen, maar ook des te minder nitraat en fosfaat kan ontstaan;
-
Stroming is een belangrijke factor in een zeeaquarium. Het doel is om zoveel mogelijk te voorkomen dat overtollig voer en ontlasting neerslaan en daarmee direct ter beschikking komen van bacteriën. Veel stroming is niet moeilijk te realiseren, een goede stroming is lastiger. Een goede stroming zorgt ervoor dat onopgeloste stoffen blijven ‘zweven’ in het water en hiermee maximaal ter beschikking staan voor opname door de dieren. Ook de beschikbaarheid voor afschuiming wordt hiermee positief beïnvloed;
-
Een goede afschuiming is van belang. Zorg voor een capabele afschuimer en zorg dat deze goed onderhouden wordt. De venturi dient regelmatig met (osmose)water te worden schoongespoeld van zoutaanslag om een goede luchtdoorstroming te behouden. Vettige aanslag in de stijgbuis van de schuimbeker belemmert de schuimvorming en dient dan ook regelmatig (minstens 1 keer per week) te worden gereinigd. Verdere aandachtspunten van goed afschuimeronderhoud zijn een schoon pomphuis, schoepenrad en magneet. Vergeet ook de binnenzijde van de afschuimer niet: de hier optredende aanslag heeft een negatieve invloed op fijnheid van luchtbelletjes;
-
Het gebruik van een fosfaatverwijderaar is ten allen tijde raadzaam en de enige manier om het systeem fosfaatarm te houden. Vele soorten zijn verkrijgbaar, de meeste op ijzerbasis. Het merk maakt niet uit; wel is het belangrijk deze goed toe te passen (geforceerde doorstroming) en deze tijdig te verversen. Wacht niet tot fosfaat meetbaar is, maar houdt een vast schema aan. Liever een niet volledig verzadigde portie weggooien, dan de ontwikkeling van AWZ te stimuleren.
In een visloos of visarm systeem zal het gemakkelijk zijn om de gewenste lage nitraat- en fosfaatwaarden te realiseren en in stand te houden. In zwaarbelaste systemen (veel en/of ‘hongerige’ vissen, koralen met specifieke voedselbehoeften) zal dit lastiger, zo niet ondoenlijk blijken, met name op het punt van nitraat.
4. Hoe werkt de wodka-methode?
Nitraat- en fosfaatoverschotten zijn te wijten aan een tekort aan koolstof. De werking van de wodka-methode is gebaseerd op het ‘herstellen’ van de stoffenbalans in de richting van de Redfield-ratio. Anders gezegd, door het toedienen van koolstof (in de vorm van ethanol) is het voor bacteriën (let op: ook voor cyano-bacteriën) mogelijk om middels assimilatie meer weefsel op te bouwen (groei en deling). Hierbij worden stikstof en fosfor ingebouwd en wordt uiteindelijk minder tot geen nitraat en fosfaat uitgestoten.
Dit proces speelt zich hoofdzakelijk af op het niveau van aërobe bacteriën. Zij bevolken alle zuurstofrijke oppervlakten, zoals glas, steen, bodemmateriaal, pompen en leidingen, maar komen ook vrij in het water voor en hebben directe toegang tot voedingsstoffen.
Door deze bacteriën van extra koolstof te voorzien in een milieu waarin stikstof en fosfor voldoende beschikbaar zijn, kunnen zij groeien en vermenigvuldigen, waarbij grote hoeveelheden stikstof en fosfor worden ingebouwd. Deze stikstof en fosfor komen nu niet meer vrij als nitraat en fosfaat, ze zijn niet meer beschikbaar voor algen, wieren en zoöxanthellen. Het resultaat is dat de ontwikkeling van algen en wieren wordt geremd en in extreme gevallen kan leiden tot het wegkwijnen ervan.
Op het niveau van zoöxanthellen in het koraalweefsel speelt zich een vergelijkbaar proces af. De zoöxanthellen zijn nu nagenoeg uitsluitend afhankelijk van de stikstof en fosfor die zij toegeschoven krijgen via hun symbiosepartner. Hierdoor kunnen de zoöxanthellen zich minder snel vermenigvuldigen en neemt langzamerhand, bij de groei van het koraal, de concentratie zoöxanthellen af. Met name aan de groeipunten van acropora’s kun je goed zien dat het koraal blijft doorgroeien, terwijl de zoöxanthellen achterblijven, met als resultaat een andere kleur groeipunt.
Naast stimulering van de aërobe bacteriën worden, zij het in mindere mate, ook de anaërobe bacteriën gestimuleerd in hun groei. Onder anaërobe bacteriën verstaan we bacteriën die leven in zuurstofarme en zuurstofloze milieus. Denk hierbij in eerste instantie aan de laag onder de aërobe bacteriën (die immers alle zuurstof verbruiken), maar ook aan poriën, smalle tunneltjes, zandbodems enzovoorts waar weinig tot geen wateruitwisseling plaatsvindt. Deze bacteriën zijn in staat om nitraat of fosfaat als zuurstofbron te gebruiken om het weinige voedsel dat hun ter beschikking staat te benutten voor hun levensprocessen. Hoewel het effect van anaërobe bacteriën op nitraatverwijdering marginaal is een extra koolstofdonor in de vorm van ethanol ook op dit niveau meer dan welkom.
5: Enkele aandachtspunten
Naar aanleiding van een artikel in ‘Der Mehrwasseraquarianer’[4] en een drie-delige publicatie op www.Korallenrif.de[5] is de wodka-methode enige jaren geleden (weer) in zwang bracht. Er wordt ingegaan op de successen van het toevoegen van koolstof (ethanol): de afname van nitraat en fosfaat. Tevens wordt stilgestaan bij enkele (mogelijk optredende) negatieve bijverschijnselen[6]. Hieronder volgen een aantal aandachtspunten die van belang zijn bij het gebruik van wodka:
1. Feitelijk is het mogelijk, zonder bijzondere dingen te doen, een nitraatwaarde van maximaal 5 à 10 mg NO3/liter te realiseren (voederregime, afschuimer, stroming). De marge van 5 à 10 mg is ruim, geen enkel aquarium is hetzelfde en veel staat of valt met het voederregime, de capaciteit van afschuimer en de stroming. Fosfaat dient bij voorkeur niet of nauwelijks meetbaar te zijn. Meestal is het gebruik van een fosfaatverwijderaar een noodzaak, maar tevens ook een afdoende methode. Alleen in aquaria met een extreem hoge visbezetting of specifiek koralenbestand (voedselinput) zal het lastig zijn nitraat onder 10 mg/liter te houden.
2. Realiseer je het volgende: Ethanol wordt door alle bacteriën opgenomen, waaronder ook cyanobacteriën. Cyanobacteriën vormen een schakel tussen bacteriën en algen. Je kunt ze beschouwen als opportunisten, ze leven zowel van lichtenergie (kooldioxide als koolstofbron) als van afvalstoffen (de andere koolstofbron). In ieder aquarium zijn cyanobacteriën aanwezig. Wanneer zichtbaar sprake is van aanwezigheid van cyanobacteriën (flap) in een aquarium, verdient het de aanbeveling voorzichtig te zijn met de wodkadosering.
3. Overdosering kan leiden tot een bacteriebloei. Bacteriebloei is te herkennen aan een zichtbare groei van een slijmlaag op de ruiten en stenen en het ‘verstopt’ raken van pompen (dichtslibben van rotor/stator). In het ergste geval vertroebelt het water en treedt een zuurstofgebrek op. Dit kan in eerste instantie leiden tot sterfte van vissen en niet symbiotische koralen; uiteindelijk kan het ook fataal zijn voor symbiotische koralen.
4. De afschuimer kan meer gaan afschuimen. Groeiende bacteriën vormen veel biomassa. Binnen deze biomassa ontstaat verstikking, waarbij de bacteriefilm loslaat. Bacterievlokken worden enerzijds door koralen geconsumeerd (lijkt op Zeovit/steentjes schudden), anderzijds worden ze afgeschuimd, waarbij stikstof en fosfaat daadwerkelijk uit de kringloop worden verwijderd uit het aquarium.
5. Methanol is giftig, maak niet de vergissing gedenatureerde alcohol te gebruiken. Bij het goedkopere segment supermarkten is consumenten wodka niet duur. Op een systeem van 500 liter kost je dit een paar cent per dag. Gedenatureerde alcohol (bijmenging van methanol) biedt het risico op een “tankcrash”.
6. Het maakt niet uit op welk moment van de dag wodka wordt toegevoegd. Het kan prettig later in de avond te doseren in verband met een “drankluchtje” dat enige tijd na dosering in de kamer blijft hangen.
6. De dosering
Er van uit gaande dat het gelukt is om op ‘natuurlijke’ wijze een nitraatwaarde van 5 à 10 mg/liter te realiseren, is een dosering van 1 à 2 ml wodka 40% per 100 liter water in de regel afdoende om de nitraatconcentratie te verlagen tot een waarde kleiner dan 1.
Men kan op twee manieren starten met het doseren van wodka: defensief en progressief. Beide methoden resulteren uiteindelijk in dezelfde einddosering. Vanuit ‘veiligheidsoverwegingen’ gaat de voorkeur uit naar de defensieve methode, maar voor zij die meer risico durven nemen, wordt ook de progressieve methode beschreven.
De defensieve wodka-methode:
Bij de defensieve wodkadosering volstaat het om vanaf het begin een dosering aan te houden van 1 à 2 ml wodka 40%. Controleer de nitraatwaarde minimaal wekelijks om de veranderingen te kunnen volgen.
Bij deze lage dosering ontwikkelen de gewenste bacteriën (aëroob en anaëroob) zich gelijkmatig en evenwichtig. De ontwikkeling van de anaërobe loopt een heel stuk trager en door laag te doseren blijft de bacteriehuishouding in 'evenwicht'. Tegelijkertijd beperk je de kans op ontwikkeling van een latent aanwezige cyanoplaag.
Gebruik de eerste maand (vier weken) om de wodka te laten inwerken op het systeem en observeer goed wat er gebeurt. Maak bijvoorbeeld een foto van een koraal waarvan bekend is, dat er iets met de kleur moet gebeuren. De eerste twee weken is er over het algemeen weinig tot geen verandering waar te nemen in de nitraatwaarde. Binnen vier weken treedt normaliter een duidelijke daling in de nitraatwaarde op en deze moet dan ook meetbaar zijn. Indien dit niet het geval is kan de dosering worden verdubbeld, dus 2 à 4 ml wodka 40%/100 liter doseren. Na globaal acht weken moet het doel (nitraat < 1 mg/liter) bereikt kunnen zijn. Vanaf dit moment kun je gaan fine-tunen.
De progressieve wodka-methode:
Eigen ervaringen met deze methode ontbreken. Wat volgt is een interpretatie van de eerder vermelde publicaties op www.korallenrif.de.
Bij de progressieve wodkadosering wordt de dosering dagelijks verhoogd. Dus op dag 1 wordt 1 ml/100 liter gedoseerd, dag 2 2 ml/100 liter, op dag 10 10 ml/100 liter enzovoorts.
Bij deze oplopende dosering neemt de biomassa van de aërobe bacteriën snel toe, met een hoog risico op bacteriebloei. Derhalve is het bij de progressieve methode van belang om dagelijks de nitraatwaarde te meten. Zodra de nitraatwaarde daalt, dient ook de dosering te worden verlaagd. Een halvering van de dosering klinkt plausibel om daarna dagelijks met 1 ml af te bouwen. Laat de nitraatmeting hierin een hulpmiddel zijn.
Wegens gebrek aan eigen ervaring met progressief doseren kan geen concreet tijdspad worden vermeld. Op deze manier zal naar schatting binnen vier weken hetzelfde resultaat worden behaald als met de defensieve methode na acht weken.
Fine-tunen:
Nadat nitraat kleiner is dan 1 mg/liter (waarbij fosfaat bij voorkeur onmeetbaar is) komt het moment van fine-tunen. Met fine-tunen wordt bedoeld: het vinden van de juiste balans tussen voedselinput, koraalkleuring en wodkadosering. Eén ieder zal hierin zijn eigen observaties moeten leren interpreteren. Eén (heel) eenvoudig trucje om te weten dat het systeem niet volledig nitraatvrij is wil ik niet achterhouden: algaanslag op de ruiten. De snelheid waarin de algen terug aanslaan op de ruit na een poetsbeurt geeft een indicatie van de beschikbaarheid van nitraat in het water. Dagelijks de ruiten moeten poetsen betekent te veel nitraat (zelfs als het niet meetbaar is), 1x per week de ruit moeten poetsen betekent dat je aan de gevaarlijk lage kant zit voor wat betreft de beschikbaarheid van nitraat.
Andere indicatoren die kunnen worden gebruikt voor het vinden van de balans zijn het te bleek worden van bijvoorbeeld montiporaplaten en het vaal kleuren van groeipunten.
Aan heel veel LPS-koralen zie je bijna niets veranderen (de Euphyllia's kleuren er niet beter of slechter van, een blaasjeskoraal kleurt wel lichter)
Bij twijfel kan men de dosering een dag overslaan of verder afbouwen.
7: Tot slot
Het gemiddelde gemengd rifaquarium kent een overschot aan nitraat en fosfaat door de hoeveelheden voedsel die wij toedienen en de ongebalanceerde samenstelling van dit voedsel. Bruinkleuring, algen en wieren kunnen hiervan het gevolg zijn. Een ervaren aquariaan weet met behulp van voederregime, stroming en afschuiming lage nitraat- en fosfaatwaarden te realiseren. De wodka-methode is een eenvoudige methode om meetbaar nitraat (en fosfaat) te bestrijden. Hiermee kan de groei van algen, wieren en zoöxanthellen worden beperkt en de kleur van voornamelijk sps-koralen worden versterkt.
Men dient zich te realiseren dat, bij het nutriënt arme milieu dat op deze manier wordt gecreëerd, koralen voedsel te kort kunnen komen. Het bijvoeren van koralen kan noodzakelijk zijn. Hierbij kan gedacht worden aan aminozuren, cyclopeeze, stofvoer, maar bedenk dat de ontlasting van vissen de koralen ook als natuurlijke voedingsbron dient.
Het blijft een complexe samenhang en het vinden van een juist evenwicht is veelal een gevoelsmatig proces - geen aquarium is hetzelfde.
[1] Koralle nr. 48 blz 68, Dezember/Januar 2007/2008, Jahrgang 8(6): fytoplankton 108:15,5:1, zoöplankton 103:16,5:1, bentische algen 550:30:1, Great Barrier Reef (plaatselijk) 1120:30:1, zoöxanhtellen in Tridacna gigas 303:52:1, chlorofyl b bevat verhoudingsgewijs meer stikstof dan chlorofyl c enzovoorts.
[2] 0,015 mg PO42-/molmassa 94,97 = 0,000158 mol PO42- = 0,000158 mol P * 16N = 0,002527 mol N = 0,002527 mol NO3- * molmassa 62,004 = 0,157 mg NO3-.
[3] Bijvoorbeeld Salifert, dubbele gevoeligheid < 0,015 mg/liter
[4] Der Mehrwasseraquarianer, nr. 1, 2004
















